Elaborato da IP Mauro NOVACCHI Unita’ Operativa di Otorinolaringoiatria – ASS 2 ‘Isontina’ – Monfalcone
ESPERIENZE DI NUTRIZIONE ENTERALE ARTIFICIALE
Il problema nutrizionale e metabolico nei pazienti sottoposti ad interventi sia sul collo (laringectomie totali, laringectomie parziali, laringectomie ricostruttive, ecc.) che del cavo orale, è molto delicato e importante in quanto influenza i tempi e le qualità del recupero post operatorio.
Vi sono ancora altre condizioni particolari che si verificano specie in pazienti affetti da neoplasie non operabili in cui sia il tipo di paziente che la necessità di un trattamento prolungato creano particolari difficoltà nella impostazione di una corretta alimentazione.
Il programma nutrizionale del soggetto che deve essere sottoposto ad intervento chirurgico importante prevede un approccio complesso, poiché nella maggioranza dei casi ci troviamo a fronteggiare una ipo e/o una malnutrizione. L’esame generale inclusi i dati antropometrici, il controllo di alcuni valori ematici significativi e una accurata anamnesi, con particolare riferimento alle abitudini alimentari e voluttuarie del paziente ed all’esistenza di affezioni metaboliche, endocrine, gastroenteriche e renali, permettono di ottenere un indice nutrizionale in modo da poter impostare, se necessaria, una dieta ipercalorica; questo sia per aumentare le difese dell’organismo che per limitare i problemi di stress derivanti dall’intervento.
Nei pazienti trattati chirurgicamente, l’alimentazione inizia nella prima giornata postoperatoria con preparati scelti tra quelli che meglio si adattano alle loro condizioni generali, fornendo comunque un surplus calorico che in molti casi raggiunge il 60% del fabbisogno basale.
L’estrema cura usata nella somministrazione con particolare riguardo alla velocità, sterilità delle manovre e corretta manutenzione del sondino naso-gastrico, hanno permesso di portare alla quasi totale assenza di problemi gastroenterici (vomito, diarrea, tensione addominale) dovute all’inquinamento dei prodotti alimentari.
Il dato più importante e che comunque maggiormente ci interessa, riguarda la limitazione, entro valori più che accettabili, della perdita di peso postoperatoria equivalente a circa il 4-5% del peso corporeo, valori che sono in linea con quelli generalmente proposti dalla letteratura.
Il nostro impegno in campo nutrizionale non si limita al trattare solo questa tipologia di pazienti, infatti con la consulenza essenziale del dietista, siamo in grado di confezionare diete speciali con l’impiego, ove richiesto, di integratori sia calorici che proteici a persone affette da altre patologie del cavo oro-faringeo (es. traumi facciali, stomatiti, ascessi peritonsillari, ecc.); sempre con questi prodotti possiamo garantire, salvo particolari controindicazioni, l’alimentazione nella stessa giornata dell’intervento a tonsillectomizzati, operati ai seni paranasali, ecc., limitando più in generale ai soli casi di necessità il digiuno prolungato.
MATERIALI E MISCELE NUTRIZIONALI
La realizzazione della nutrizione enterale prevede l’impiego di materiali specifici che comprendono:
SONDE NUTRIZIONALI
Questo tipo di materiale può essere considerato ideale quando permette un trattamento nutrizionale con il massimo comfort del paziente senza effetti collaterali e quando può rimanere in sede anche per lungo tempo.
La sonda ideale dovrebbe essere:
biologicamente inerte: non provocare cessione di agenti tossici
resistere all’azione dei succhi gastroenterici
idrorepellente: la miscela nutritiva non deve aderire alle pareti interne
resistere alla trazione longitudinale ed alla pressione endoluminale
morbida e flessibile
di piccole dimensioni
con un rapporto esterno/interno il più elevato possibile
Nel corso degli ultimi anni i progressi tecnologici, hanno permesso di ottenere materiali con caratteristiche molto vicine a quelle richieste per realizzare una sonda ideale. Sono stati abbandonati i materiali quali la gomma e polivinilclorulo (PVC) responsabili di numerose complicanze legate al loro contatto con l’apparato digerente. Attualmente i materiali più comuni sono silicone e poliuretano, ognuno dei quali con peculiarità proprie, che permettono la realizzazione di sonde che hanno all’incirca la stessa efficacia clinica.
Queste ultime vengono realizzate con caratteristiche diverse fra loro, in funzione della via d’accesso (nasogastrica, nasodigiunale, faringostomica, gastrostomica, digiunostomica) al tratto gastroenterico:
dimensioni: espresse in FRENCH (1 French = 0,33 mm)
radiopacità, lunghezza, fori d’uscita
tipo di collegamento con il resto del sistema infusionale (luer-lock o universale)
tacche di riferimento per la lunghezza
presenza di un peso alla punta
presenza di un lubrificante già incorporato
Ai nostri pazienti vengono posizionali, in linea di massima, sondini in poliuretano e più raramente sondini in silicone.
CONTENITORI E DEFLUSSORI
La somministrazione delle miscele nutrizionali può avvenire:
tramite siringhe: in pochi minuti può essere somministrato un “bolo” di 200-400 ml di miscela nutrizionale. La somministrazione viene ripetuta ad intervalli di 4-6 ore durante la giornata. Anche se apparentemente questa tecnica si avvicina ai ritmi fisiologici della normale alimentazione, non è sicura da rischio di effetti collaterali (tensione addominale, nausea, diarrea), specie se la somministrazione avviene nelle anse digiunali. Inoltre, causa il maggior numero di manipolazioni necessarie, aumenta il rischio di contaminazione batterica.
direttamente dai contenitori di miscela (flaconi di vetro o barattoli) con l’utilizzazione di deflussori ad essi adattabili. La disponibilità di questo sistema ha il vantaggio di evitare i costi aggiuntivi legati all’impiego della sacca nutrizionale. D’altro canto il volume di miscela in ogni contenitore originale è di per se insufficiente a soddisfare tutte le richieste nutrizionali e pertanto questo sistema di somministrazione richiede più sostituzioni nell’arco della giornata e quindi più lavoro e controllo. Inoltre le ripetute manipolazioni sulla linea infusionale possono aumentare l’incidenza di contaminazione microbica.
con l’uso di “sacche nutrizionali” che permettono di ridurre al minimo il numero di manipolazioni lungo la linea infusionale. Le sacche devono essere di materiale che non determini la cessione di agenti tossici (es. EVA) e devono essere realizzate con criteri che rendano il loro riempimento il più semplice e sicuro possibile.
Le capacità di collabire delle pareti delle sacche, man mano che la miscela scende, impedisce il contatto continuo con l’aria (come si ha invece con i contenitori di vetro) creando un sistema chiuso e garantendo quindi una minore incidenza di contaminazioni microbiche.
E’ importante a questo punto sottolineare come qualsiasi manipolazione della linea infusionale e le procedure di riempimento delle sacche debbano essere eseguite, se non in tecnica asettica come per la parenterale, certamente dopo idoneo addestramento e con tecniche che prevedano la più rigorosa pulizia delle zone di lavoro e dell’operatore.
POMPE INFUSIONALI O NUTRIPOMPE
Lo scopo di una nutripompa è quello di garantire la costanza del flusso della miscela durante il periodo di infusione.
In questo modo vengono evitati quegli inconvenienti legati alla somministrazione per gravità, quali:
per eccessiva velocità: distensione addominale, crampi, diarrea, nausea
per rallentata velocità: ridotta introduzione di nutrienti, rischio di ostruzione della sonda.
L’uso di nutripompe riduce i tempi di assistenza, migliora il comfort del paziente e l’efficacia terapeutica.
Le pompe hanno di solito alcune caratteristiche fondamentali:
alimentazione in rete e a batterie ricaricabili
leggerezza, trasportabilità, silenziosità
sistemi di allarme
appositi set infusionali collegabili o già collegati ai contenitori delle miscele nutrizionali
semplicità d’uso
PULIZIA E MANUTENZIONE DELLE POMPE ENTERALI
Le pompe per la nutrizione enterale di cui disponiamo in reparto sono del tipo Flexiflo II della ditta Abbot, questo tipo di pompe da quanto abbiamo avuto modo di constatare necessita di poca manutenzione.
Il sistema resiste alla fuoriuscita di liquido dalla linea, anche se per un buon funzionamento è consigliabile controllare giornalmente la pompa e rimuovere eventuali perdite di soluzione, sicuri che una adeguata pulizia assicurerà il costante e corretto funzionamento
Per il lavaggio si può utilizzare dell’acqua tiepida saponata; la parte superiore della pompa può essere staccata ed immersa in acqua (supporto del flexitainer), la parte inferiore non può essere immersa e pertanto va lavata con una spugnetta. Controllare con attenzione l’area di inserzione della capsula volumetrica e, se necessario, rimuovere le tracce di soluzione con uno spazzolino.
MISCELE NUTRIZIONALI
La loro scelta appropriata permette di soddisfare i fabbisogni qualitativi e quantitativi dei singoli pazienti.
Possiamo distinguere:
Diete naturali artigianali.
Preparati con alimenti naturali trasformati in forma liquida o semiliquida.Accanto al vantaggio di essere “naturali e poco costose”, annoverano numerosi inconvenienti:
scarsa omogeneità e fluidità, che obbligano all’impiego di sonde nutritive di ampio calibro
osmolarità spesso elevata
composizione bromatologica non precisabile, spesso incompleta come vitamine, oligoelementi, minerali
maggior rischio di contaminazione durante la preparazione
presenza di grosse quantità di aria.
Queste diete richiedono l’integrità di tutti i processi digestive e di assorbimento ed il loro uso è consigliabile solo in situazioni organizzative peculiari che permettano il loro controllo bromatologico e batteriologico.
Diete naturali “Industriali”.
Esistono diete a base di alimenti naturali, ma a preparazione industriale (es. NUTRODRIP) ottenute mediante processi di omogeneizzazione controllati. Vengono in questo modo superati la maggior parte dei problemi delle diete naturali artigianali, perché queste diete:
Possono essere somministrate con sondini di piccolo calibro
sono isoosmolari
Hanno una composizione nota ed equilibrata
Sono in confezioni sterili e pronte per l’uso
Sono praticamente prive di lattosio, a basso contenuto di sodio e di colesterolo
Contengono fibre indigeribili
Diete chimicamente definite.
polimeriche: contengono proteine intere come fonte azotata (albume d’uovo o proteine del latte), maltodestrine e oli vegetali e trigliceridi a media catena (MCT) come fonte energetica. Sono prodotti in forma liquida pronti all’uso, sterili e, più raramente, in polvere (da ricostruire). I nutrienti presenti sono in rapporti equilibrati e noti, inoltre necessitano di solo una parte dei processi digestivi. Queste diete sono quindi indicate per tutti i pazienti con funzionalità gastroenterica integra o parzialmente compromessa. La maggior parte di queste diete ha una densità calorica di 1 cal/ml alcune, pur mantenendo le stesse caratteristiche, sono formulate per fornire 1,5 Cal/ml.
Monomeriche o elementari/semielementari: costituite da nutrienti allo stato semplice, in pratica pronti per l’assorbimento, essenzialmente per quanto riguarda la fonte azotata. Possono essere presente aminoacidi liberi (monomeriche o elementari) per il cui assorbimento non è richiesta l’idrilisis enzimatica o miscele di aminoacidi e peptidi a piccola catena (semielementari), la cui presenza ha il vantaggio di ridurre l’elevata osmolarità delle monomeriche e di non impegnare comunque l’apparato digerente.
Queste diete hanno indicazioni in casi molto selezionati di pazienti con gravi deficit digestivi. La componente energetica è la stessa delle diete polimeriche.
Diete modulari o integratori dietetici: nonostante la grande varietà di diete enterali disponibili, in alcuni pazienti può esserci la necessità di variare l’apporto di uno o più nutrienti rispetto alla formulazione abituale o, in caso di nutrizione per os, rispetto all’alimentazione naturale residua.
Per questi pazienti sono disponibili prodotti dietetici contenenti nutrienti singoli o comunque in proporzioni non equilibrate.
Essi possono essere somministrati separatamente, ad integrazione di una normale alimentazione comunque insufficiente a coprire tutte le necessità. Oppure direttamente miscelati nella sacca nutrizionale in caso di NE.
Ovviamente la quantità e la qualità di una dieta modulare o di un integratore deve essere stabilita per singolo paziente.
POSIZIONAMENTO DEL SONDINO NASO GASTRICO
La procedura di posizionamento del sondino è una manovra relativamente semplice, la semplicità è comunque legata al tipo di materiale utilizzato e dal grado di cooperazione del paziente.
Se il paziente è cosciente risulta fondamentale cercare di tranquillizzarlo e guadagnarsi la sua collaborazione spiegando la procedura di posizionamento e le azioni che gli verranno richieste per rendere più agevole e rapida l’operazione.
Per il posizionamento dei sondini si procede nel seguente modo:
Il paziente viene posto in posizione seduta (90°) o semiseduta (30°), la posizione su un fianco è la meno indicata.
Esaminare le fosse nasali per verificare l’esistenza di ostruzioni meccaniche; far inspirare il paziente con il naso e chiudendo alternativamente una narice, scegliere per l’introduzione quella più ampia.
Determinare la porzione del sondino da inserire (1 tacca=50 cm)
Lubrificare il sondino (i sondini da noi utilizzati non abbisognano di essere lubrificati, basta bagnare con acqua la porzione di sondino che verrà introdotta)
Introdurre delicatamente la punta del sondino nelle narice prescelta facendola scivolare sul pavimento della fossa nasale. Dopo l’introduzione di 7-10 cm l’estremo viene a trovarsi in rinofaringe, a questo punto ruotare il sondino di 180° e chiedere al paziente di iniziare a sorseggiare acqua e deglutire.
Continuare a far scorrere il sondino fino alla lunghezza calcolata senza cercare di forzare l’inserimento qualora si incontrasse resistenza, ritirare il sondino e ritentare delicatamente il passaggio. Un accidentale posizionamento in trachea normalmente induce tosse o soffocamento. Se il sondino si trova in laringe, il paziente sarà impossibilitato a parlare per cui sarà opportuno accordarsi in anticipo su un segnale con le mani che indichi, qualora si presenti senso di disagio o difficoltà respiratoria, di fermare l’operazione.
N.B. quando si usano sondini molto sottili tali sintomi possono non essere immediatamente osservabili.
Con il sondino posizionato per tutta la lunghezza desiderata, bisogna verificare il corretto posizionamento nel seguente modo:
aspirare il contenuto gastrico con una siringa e verificare la natura osservandone le caratteristiche (conferma del pH acido con cartina al tornasole)
con un siringone da 60 cc iniettare attraverso la sonda 20-25 cc di aria, auscultando contemporaneamente con un fonendoscopio sul quadrante addominale superiore sinistro; l’entrata dell’aria nello stoma produce un tipico brontolio;
con sondino radiopaco come quelli da noi utilizzati, in caso di dubbio sul posizionamento si può ricorrere al controllo radiografico.
Il sondino deve essere fissato al viso del paziente con cerotto possibilmente anallergico assicurandosi di non determinare pressioni o distorsioni delle narici. Nel nostro reparto il sondino viene fissato al naso. Il cerotto deve essere sostituito ogni qualvolta si allenti, è comunque buona regola cercare di far ruotare il punto di applicazione per prevenire irritazioni della pelle.
Dopo aver terminato la procedura di posizionamento, il paziente deve essere tenuto in osservazione per eventuali difficoltà respiratorie o dolori addominali per almeno 30-60 min. prima di iniziare l’alimentazione.
Il sondino deve essere lavato con acqua (25-100 ml) al termine di ogni somministrazione in caso di nutrizione intermittente (bolo), oppure ogni 3-6 ore in caso di nutrizione continua. Questa manovra permette di prevenire l’intasamento e di fornire supplementi di acqua. Durante le pause dell’alimentazione chiudere il connettore per evitare l’inquinamento del sondino e l’inversione di flusso dei succhi gastrici.
Prima delle somministrazioni dei nutrienti controllare il corretto posizionamento della sonda.
SONDA NASO GASTRICA: complicanze meccaniche.
COMPLICANZE: Riniti-faringiti erosione mucosa esofagea
POSSIBILI CAUSE: Uso di sonde di grosso calibro in materiale non biocompatibile
ACCORGIMENTI PREVENTIVI E TERAPEUTICI: Sonde di piccolo calibro in poliuretano, Sylastic e C-flex
COMPLICANZE: Ostruzione della sonda
POSSIBILI CAUSE: Miscela nutritiva densa poco omogenea, farmaci somministrati ACCORGIMENTI PREVENTIVI E TERAPEUTICI: attraverso la sonda Accurata preparazione della miscela nutritiva, frequenti lavaggi con acqua uso di pompa peristaltica
COMPLICANZE: Reflusso gastro-esofageo, aspirazione tracheo-bonchiale
POSSIBILI CAUSE: Deficit di svuotamento, infusione troppo rapida posizione del ACCORGIMENTI PREVENTIVI E TERAPEUTICI: paziente Posizionamento del paziente seduto o semiseduto; somministrazione oltre al piloro
COMPLICANZE: Dislocazione della sonda
POSSIBILI CAUSE: Vomito, tosse
ACCORGIMENTI PREVENTIVI E TERAPEUTICI: Accurato fissaggio della sonda al naso, riposizionamento della sonda, controllo radiografico
PROTOCOLLO PER L’ALIMENTAZIONE ENTERALE POST OPERATORIA
Prima di aprire o travasare i prodotti, lavarsi accuratamente le mani, è opportuno l’uso dei guanti monouso e copricapi in maniera di ridurre il rischio di contaminazione
Preparare la dieta in ambiente isolato dal reparto di degenza e refrigerarla sino al momento dell’uso
I prodotti possono essere diluiti con acqua a meno che non siano previsti prodotti sterili
se si usano bottiglie da 300 ml: infilarla nel supporto, togliere il tappo e sostituirlo con il set di somministrazione;
se si usa una sacca di 1000 ml: aprire le bottiglie o le lattine (dopo averle sciacquate con acqua ed asciugate) e versare il contenuto nel contenitore, richiudere il contenitore con l’apposito tappo o connettervi l’apposito set di somministrazione; contrassegnare i prodotti aperti con data e ora di apertura, coprirli e conservarli in frigorifero per non più di 24 ore; attaccare alle sacche un’etichetta autoadesiva con il nome del paziente, il tipo, la quantità e velocità della dieta prescritta.
N.B. i prodotti diluiti con acqua non sono sterili e devono essere utilizzati entro breve tempo.
L’aggiunta alla dieta di altri elementi specie se in polvere, deve essere fatta subito prima dell’uso
Prima di ogni somministrazione controllare il posizionamento del sondino
Controllare il volume dei residui gastrici, se superiori ai 150 ml indagare sulle cause del ritardato svuotamento gastrico ed eventualmente variare lo schema di somministrazione
Durante l’alimentazione e per almeno 30’ dopo il termine del pasto il paziente deve stare in posizione seduta o semiseduta (30°)
L’alimentazione va iniziata nelle prime giornate lentamente; evitare di aumentare contemporaneamente flusso e concentrazione della miscela e qualora si presentino segni di intolleranza quali diarrea, nausea e glicosuria ritornare a concentrazioni e flussi precedentemente tollerati
Al termine della somministrazione della dieta eseguire la pulizia della sonda con 25-10 ml di acqua
Sostituire ogni 24 ore il contenitore ed il set di somministrazione
Non aggiungere altri elementi a quello già presente nel sistema di alimentazione
Ridurre al minimo le aperture del sistema in corsia
Annotare la durata del pasto, la quantità di miscela somministrata, il volume di supplementi d’acqua ed ogni reazione del paziente
Prendere tutte le misure necessarie a prevenire l’inalazione degli alimenti
Rilevare i parametri di valutazione della risposta del paziente alla N.E.T.
peso corporeo (prima dell’inizio del trattamento e quindi ogni giorno sino al suo termine
aspetto della pelle, degli occhi, della lingua e mucose (giornalmente)
controllo elettroliti serici ed ematocrito (giornalmente per i primi quattro giorni dopo l’intervallo e quindi a giorni alterni)
controllo reticolociti, sideremia e TIBC in prima giornata e successivamente ogni sette giorni
controllo elettroforesi in decima giornata
urine (giornalmente per i primi quattro giorni dopo l’intervallo e successivamente a giorni alterni)
risposta gastro intestinale (in caso di stitichezza dovuta a deficit d’azione del torchio addominale, somministrare blandi lassativi come il levulosio, in caso di insuccesso, previa prescrizione medica, clistere evacuativo max 1000 cc.)
BIBLIOGRAFIA
G. Negri, P. Zannini “Le vie di somministrazione enterale”
2° Corso Nazionale “Il nursing in ORL” , Bologna
G. Perfumo, M. Toscano, S. Righi “L’alimentazione nel decorso post operatorio”
M. Piemonte – XIII Convegno Nazionale “La riabilitazione dopo grande chirurgia del collo”
IP-AFD Giorgio Cantarut, IP Mauro Novacchi “Aggiornamento in ORL” Atti ASS 2 Isontina


 laringoscopia indiretta: consiste nella visualizzazione della laringe tramite uno specchietto; è l’esame che si ese
laringoscopia indiretta: consiste nella visualizzazione della laringe tramite uno specchietto; è l’esame che si ese laringoscopia con fibre ottiche: consiste nella visualizzazione della laringe attraverso una piccola telecamera situata all’interno di un fibroscopio, uno strumento sottile e flessibile che viene introdotto attraverso il naso per arrivare in stretta prossimità della laringe stessa;
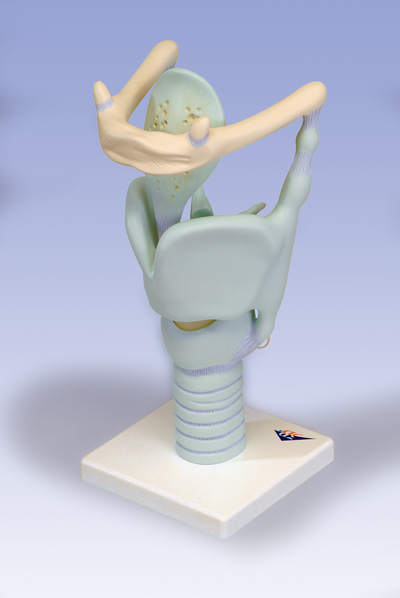
laringoscopia con fibre ottiche: consiste nella visualizzazione della laringe attraverso una piccola telecamera situata all’interno di un fibroscopio, uno strumento sottile e flessibile che viene introdotto attraverso il naso per arrivare in stretta prossimità della laringe stessa; laringoscopia in sospensione: è l’esame più valido per la diagnosi definitiva; permette di effettuare la biopsia della lesione sospetta (prelievo di tessuto per l’analisi microscopica) e a volte consente di eseguire interventi chirurgici risolutivi in presenza di lesioni iniziali che interessano una piccola porzione delle corde vocali o di altri
laringoscopia in sospensione: è l’esame più valido per la diagnosi definitiva; permette di effettuare la biopsia della lesione sospetta (prelievo di tessuto per l’analisi microscopica) e a volte consente di eseguire interventi chirurgici risolutivi in presenza di lesioni iniziali che interessano una piccola porzione delle corde vocali o di altri
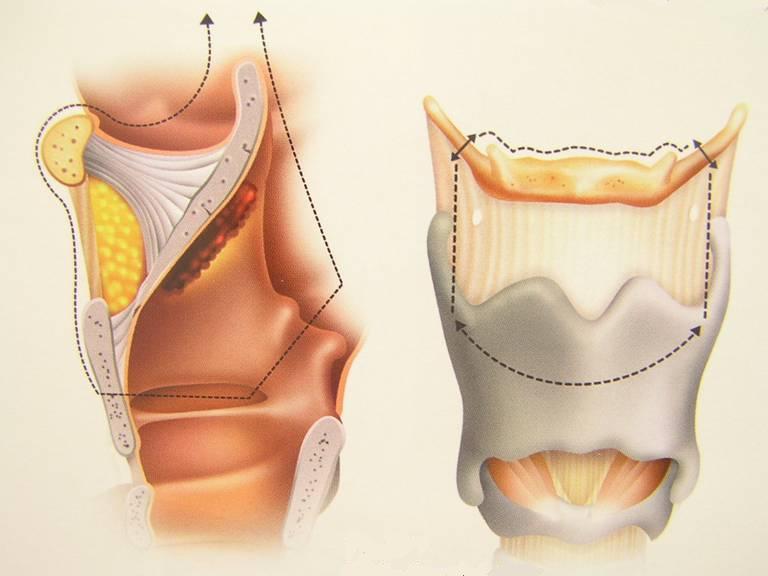
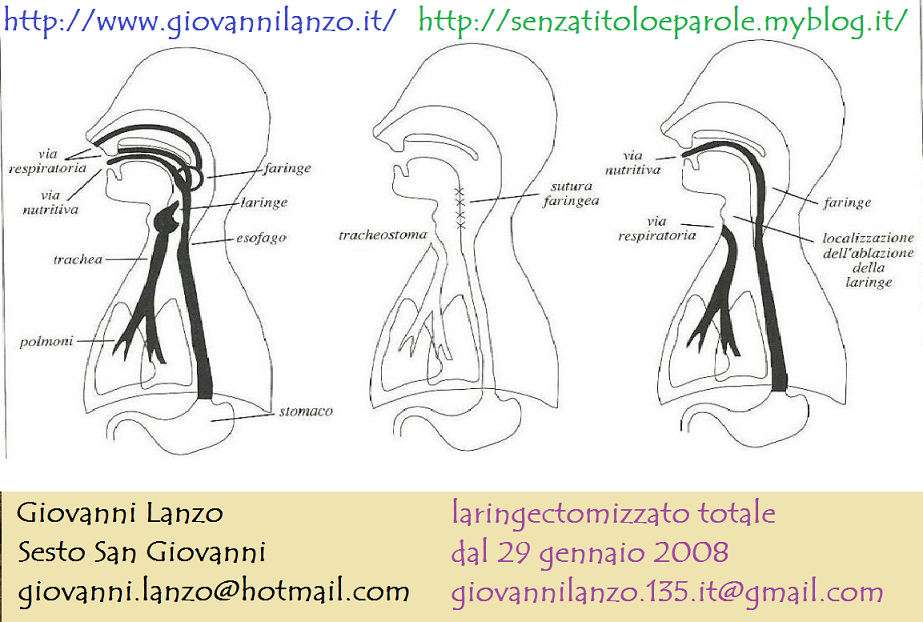
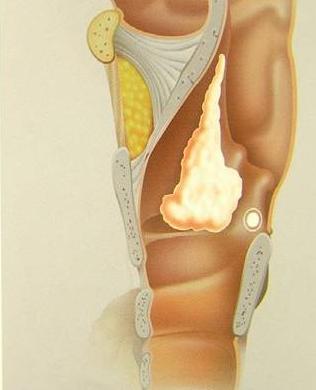
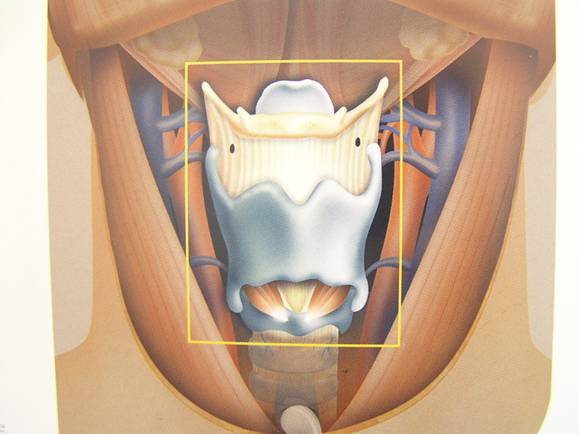 laringectomia totale: si esegue nelle fasi più avanzate del tumore nel caso non fosse possibile conservare l’unità funzionale minima della laringe, non necessariamente per l’estensione del tumore ma anche nei casi in cui vi fosse interessamento di alcuni punti critici della laringe, anche in presenza di una neoplasia non troppo estesa. In questi casi il tracheostoma è definitivo come pure la perdita della voce naturale ma paradossalmente il periodo post-operatorio è molto meno impegnativo per il paziente visto che non è necessario il periodo di rieducazione per la ripresa delle funzioni della laringe.
laringectomia totale: si esegue nelle fasi più avanzate del tumore nel caso non fosse possibile conservare l’unità funzionale minima della laringe, non necessariamente per l’estensione del tumore ma anche nei casi in cui vi fosse interessamento di alcuni punti critici della laringe, anche in presenza di una neoplasia non troppo estesa. In questi casi il tracheostoma è definitivo come pure la perdita della voce naturale ma paradossalmente il periodo post-operatorio è molto meno impegnativo per il paziente visto che non è necessario il periodo di rieducazione per la ripresa delle funzioni della laringe.

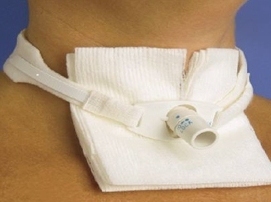 Il tracheostoma rappresenta la nuova via di passaggio dell’aria durante la respirazione. Non è necessario alcun controllo da parte del paziente che dovrà semplicemente respirare come prima dell’intervento chirurgico.
Il tracheostoma rappresenta la nuova via di passaggio dell’aria durante la respirazione. Non è necessario alcun controllo da parte del paziente che dovrà semplicemente respirare come prima dell’intervento chirurgico.


