Archivio tag: anatomia
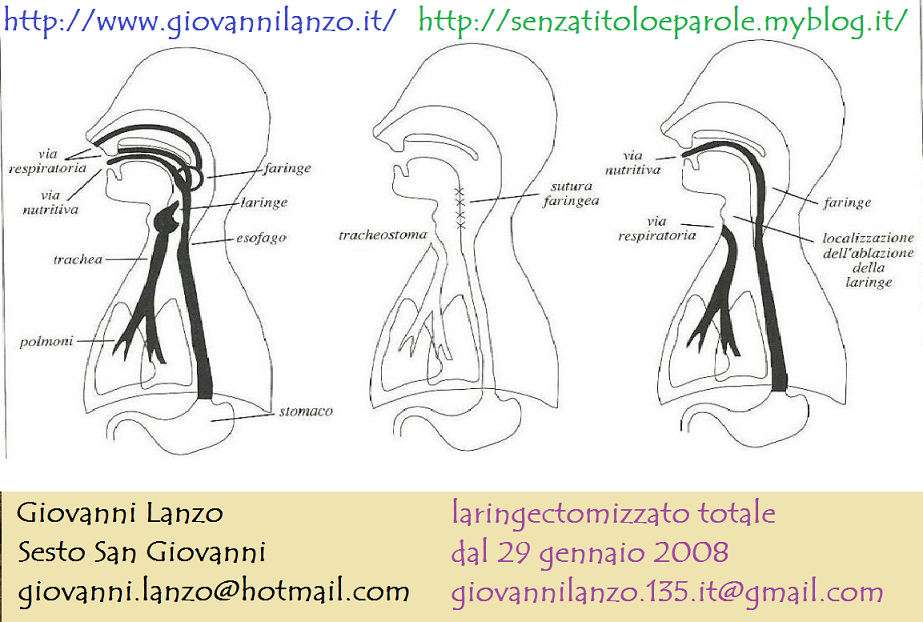
Il ritorno a casa-Anatomia e fisiologia della laringe
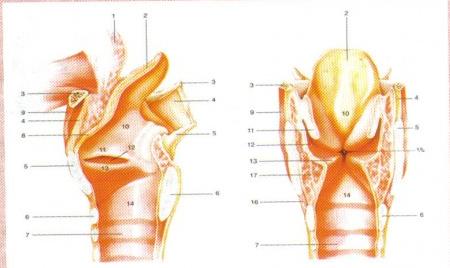
LARINGE-Richiami anatomici
|
Sezione sagittale della laringe:
|
 |
Sedi e sottosedi (UICC)
|
Sovraglottide I Epiglottide sovraioidea |
Glottide I Corde vocali |
Sottoglottide |
Richiami di anatomia patologica
La maggior parte dei carcinomi laringei è costituita da carcinomi squamocellulari; tuttavia in tale sede anatomica è possibile l’insorgenza di numerosi altri istotipi (vedi tabella pag 12) la cui precisa identificazione riveste notevole importanza anche a fini terapeutico- prognostici.
Evoluzione locale
Avviene seguendo precise vie di diffusione a causa della coesistenza nella laringe di aree di maggiore e minore resistenza nei confronti della progressione tumorale. Ci sono barriere anatomiche che riescono ad ostacolare l’estensione extralaringea del tumore, per esempio le cartilagini tiroidea e cricoidea, la membrana io- epiglottica, la membrana io- tiroidea. Rappresentano invece aree di minor resistenza la commessura anteriore, la membrana cricotiroidea, gli orifizi cribriformi dell’epiglottide.
Evoluzione regionale
La laringe sovraglottica ha una ricca rete linfatica sottomucosa. Le percentuali di metastasi linfonodali variano dal 15% al 51% relativamente alla classe ed alla sede del tumore primitivo. La laringe glottica ha una scarsa rete vascolare e linfatica, pertanto le neoplasie di questa sede hanno scarsa tendenza alla metastatizzazione. La laringe sottoglottica è fornita di una ricca rete linfatica drenante nei linfonodi giugulari inferiori o paratracheali
Evoluzione a distanza
Le metastasi si verificano nel 5- 10% dei casi, per lo più al polmone ed eccezionalmente all’osso e al fegato.
Iter diagnostico
La sintomatologia è rappresentata da disfonia per i tumori glottici; senso di corpo estraneo, disfagia e otalgia riflessa per i tumori sovraglottici; dispnea inspiratoria per i tumori glotto-sottoglottici e più raramente per i tumori sovraglottici. Per la diagnosi del tumore primitivo si utilizzano:
- la laringoscopia indiretta con specchietto tradizionale o con fibroscopia ad ottiche rigide o flessibili che consente di valutare la morfologia e la motilità laringea;
- la laringoscopia diretta in narcosi che consente un esame più particolareggiato e l’esecuzione del prelievo bioptico;
- l’imaging (TC e RM) che fornisce informazioni dettagliate riguardanti l’infiltrazione in profondità. La TC è sufficiente ad assicurare la programmazione di un piano terapeutico adeguato, la RM può essere utilizzata in modo più limitato come mezzo problem-solving.
Devono essere inoltre valutati fattori relativi al paziente (performance status, funzionalità dell’apparato respiratorio, presenza di tumori sincroni delle vie aerodigestive superiori) e fattori relativi alla neoplasia (estensione, motilità cordale, infiltrazione della commessura anteriore, sconfinamento sottoglottico, coinvolgimento aritenoideo, estensione al ventricolo di Morgagni, invasione dello spazio paraglottico, infiltrazione cartilaginea, invasione metastatica linfonodale).
Classificazione di T (UICC, 1997)
T0 Tumore primitivo non evidenziabile
Tis Carcinoma in situ
Sovraglottide
| T1 | Una sola sottosede, con mobilità normale delle corde vocali |
| T2 | Più di una delle sottosedi adiacenti della sovraglottide o della glottide o regioni esterne alla sovraglottide (ad es. base della lingua, vallecula, parete mediale del seno piriforme) senza fissazione della laringe |
| T3 | Limitato alla laringe con fissazione della corda vocale e/o invasione di una qualsiasi delle seguenti strutture: area postcricoidea, tessuti pre-epiglottici, base profonda della lingua |
| T4 | Invasione della cartilagine tiroidea e/o estensione nei tessuti molli del collo, nella tiroide e/o nell’esofago |
Glottide
| T1 | Corda(e) vocale(i) (può coinvolgere la commissura anteriore o quella posteriore) con normale mobilità (T1a: una sola corda vocale; T1b: entrambe le corde vocali) |
| T2 | Estensione alla sovraglottide e/ o alla sottoglottide, e/o con compromissione della mobilità cordale |
| T3 | Limitato alla laringe con fissazione delle corde vocali. |
| T4 | Invasione della cartilagine tiroidea e/ o estensione in altri tessuti al di là della laringe, ad esempio trachea, tessuti molli del collo, tiroide, faringe. |
Sottoglottide
| T1 | Limitato alla sottoglottide. |
| T2 | Estensione a una o entrambe le corde vocali, con mobilità normale o compromessa. |
| T3 | Limitato alla laringe con fissazione delle corde vocali. |
| T4 | Invasione della cartilagine cricoidea o tiroidea e/ o estensione in altri tessuti al di là della laringe, ad esempio trachea, tessuti molli del collo, tiroide, esofago. |
Terapia
Tipi di intervento chirurgico
Tumore primitivo: il trattamento chirurgico dei carcinomi laringei si avvale di tecniche funzionali o demolitive. I tumori sovraglottici possono essere trattati con laser-chirurgia ed epiglottectomia se di piccole dimensioni oppure con laringectomia sovraglottica, eventualmente allargata alla base della lingua o al seno piriforme, per le lesioni più estese. I casi con fissità laringea richiedono una laringectomia totale. I tumori glottici in stadio iniziale possono essere trattati con cordectomia, glottectomia, laringectomia fronto-laterale, emilaringectomia, laringectomia subtotale ricostruttiva; le lesioni in stadio più avanzato possono essere sottoposte a chirurgia ricostruttiva o a laringectomia totale. I tumori sottoglottici devono essere trattati con laringectomia totale con sacrificio dei primi sei anelli tracheali.
In tutti gli interventi funzionali viene conservata la funzione respiratoria, mentre risultano parzialmente compromesse la fonazione e la deglutizione, peraltro suscettibili di miglioramento dopo rieducazione logopedica. La laringectomia sovraglottica e le laringectomie subtotali ricostruttive prevedono una compromissione della deglutizione ed un certo grado di inalazione nel postoperatorio. Per tale ragione sono controindicazioni generali a questi interventi l’età avanzata, le scadenti condizioni generali, la compromissione delle funzioni cardio-respiratorie.
La chirurgia demolitiva (laringectomia totale) comporta la perdita della funzione fonatoria e di quella respiratoria, per cui il paziente è portatore di tracheostoma permanente. L’utilizzo di protesi fonatorie o di valvole può consentire il recupero della fonazione.
Linfonodi regionali: nei tumori sovraglottici, considerando l’elevato rischio di metastatizzazione, lo svuotamento bilaterale del collo è sempre indicato e può essere di tipo selettivo per gli N0, funzionale per gli N1, di tipo funzionale, radicale modificato o radicale classico per gli N 2 e di tipo radicale classico per gli N 3.
I tumori glottici, data la scarsa tendenza alla metastatizzazione laterocervicale, consentono l’astensione dal trattamento chirurgico dei linfonodi in caso di lesione T1N0, mentre per tutte le altre classi di T è indicato lo svuotamento bilaterale selettivo per i casi N0, funzionale nei casi N 1, funzionale o radicale modificato o radicale classico nei casi N 2, radicale classico nei casi N 3.
Considerando la possibile evoluzione metastatica dei tumori sottoglottici verso i linfonodi paratracheali e verso quelli del mediastino superiore, lo svuotamento laterocervicale bilaterale deve essere di tipo funzionale o radicale, possibilmente esteso ai linfonodi mediastinici sia pure con i limiti tecnici e di radicalità che tale metodica comporta.
Radioterapia
La radioterapia è entrata a far parte delle opzioni terapeutiche per le forme iniziali, mentre per ciò che concerne il trattamento dei casi più avanzati la chirurgia rimane oggi, in Italia, il trattamento più utilizzato. La mucosite è un possibile effetto acuto, mentre tra le complicazioni (<1%) abbiamo l’edema laringeo, che può richiedere la tracheostomia e la condronecrosi.
Laringe sovraglottica: in Italia il trattamento di scelta è la chirurgia, sebbene la radioterapia possa ottenere ottimi risultati per i T1- T2 N0 vegetanti. La radioterapia è il trattamento dei casi non operabili, dei pazienti che rifiutano la chirurgia e dei casi oncologicamente non resecabili. Poichè vi è un rapporto tra positività linfonodale e stadio del tumore primitivo pari al 28% per i T1, 40% per i T2, 45% per i T3 e 73% per i T4, come riportato da Lindberg, e poichè, come riportato da Wang, i linfonodi positivi sono nel 55% dei casi i superiori, nel 29% i medi e nel 5% gli inferiori, le dimensioni dei campi di trattamento devono essere adeguate. La dose da erogare, con frazionamento tradizionale (180-200 cGy), varia da 6600 a 7000 cGy in funzione dello stadio del tumore primitivo e dell’interessamento linfonodale. Eventuali interruzioni nella erogazione della dose sono un fattore prognostico sfavorevole per ciò che concerne il controllo locale: pertanto devono essere evitate con appropriate terapie farmacologiche e con un approccio dietologico.
Laringe glottica: è ormai universalmente accettato che la radioterapia è in grado di ottenere percentuali di guarigione analoghe a quelle della chirurgia per i T1a e b della glottide. In tal senso parlano i dati della letteratura internazionale dal I Congresso Internazionale sulla laringe di Toronto (1974) sino a quello di Sidney (1994). La scelta viene fatta in genere in base alle preferenze del paziente, al tipo di lavoro del paziente, alla esperienza ed alla disponibilità della équipe curante (chirurgo e radioterapista). La qualità della voce, dopo radioterapia, è migliore di quella dopo chirurgia, anche dopo chirurgia laser. Nel trattamento dei T2 la radioterapia non consente le stesse probabilità di controllo della chirurgia. Nei paesi anglosassoni l’approccio prevalente è quello radioterapico, mentre nei paesi latini l’approccio predominante è quello chirurgico. Il trattamento dei T3 è chirurgico; sono attualmente in corso studi di associazione radio- chemioterapica con finalità di preservazione d’organo. La dose da erogare per i T1, con frazioni di 200 cGy, è compresa nel range 6400- 7000 cGy; per i T2 varia da 6200 a 7200 cGy, in funzione del sottostadio T2a o T2b; per i T3- T4 è di 7000 cGy.
Laringe sottoglottica: la radioterapia è il trattamento di scelta nelle lesioni iniziali T1 e T2 senza adenopatie clinicamente palpabili. Nel trattamento dei casi più avanzati la radioterapia trova indicazione per i casi non operabili o non resecabili.
Le dosi da erogare, con frazionamento tradizionale, variano da 6400 cGy a 7200 cGy, in funzione della sede e dello stadio del tumore. Sono in corso di valutazione i multifrazionamenti.
Indicazioni terapeutiche
Tumore primitivo
La radioterapia postoperatoria è indicata se i margini sono positivi, se esiste un’incerta radicalità chirurgica, se si reperta un’evoluzione sottoglottica, in caso di T4, N+ R+ o in caso di più di 3 linfonodi metastatici. La radioterapia postoperatoria deve essere iniziata tra le 4 e le 6 settimane dall’intervento chirurgico.
Terapia non standard: sono in corso studi clinici randomizzati di radiochemioterapia concomitante versus terapia standard, atti a valutare la possibilità di risparmio d’organo.
Tumori sopraglottici
| T1/T2 |
|
| T3/T4 operabili |
|
| T4 non resecabili |
|
| Pazienti inoperabili per ragioni internistiche |
|
Tumori glottici
| T1 |
|
| T2 |
|
| T3/T4 resecabili |
|
|
T4 |
|
| Pazienti inoperabili per ragioni internistiche |
|
Tumori sottoglottici
| T1/T2 |
|
| T3/T4 operabili |
|
| Tumori non resecabili |
|
| Pazienti inoperabili per ragioni internistiche |
|
Rete linfatica
Tumori sopraglottici
| N0 |
|
| N1 |
|
| N2 |
|
| N3 |
|
Tumori glottici (solo per T2-T3-T4)
| N0 |
|
| N1 |
|
| N2 |
|
| N3 |
|
Tumori sottoglottici (svuotamento esteso al VI livello)
| N0 |
|
| N1 |
|
| N2 |
|
| N3 |
|
Risultati
Negli stadi iniziali delle lesioni sovraglottiche con la chirurgia si ottiene dal 90% al 95% di controllo nei T1 e dall’80% al 90% nei T2; la radioterapia ottiene una percentuale di controllo variabile dall’80 al 90% nei T1 e dal 70% all’80% nei T2. Il recupero chirurgico dei fallimenti radioterapici rende simili le percentuali di controllo delle due modalità di trattamento. Le classi avanzate dei carcinomi sovraglottici hanno invece una prognosi più infausta a causa della maggiore incidenza di metastasi laterocervicali. Il controllo locale dei T3 trattati con radioterapia è del 60%; per i T4 è del 40-50%.
Il controllo locale della chirurgia sola non è ben definito, poiché molti studi includono pazienti sottoposti a trattamento combinato, e varia dal 70% al 90%. Il trattamento combinato laringectomia sovraglottica e radioterapia post- operatoria ha consentito di ottenere percentuali di sopravvivenza libera da malattia di circa l’80% a 5 anni.
Le obiezioni a questa strategia si basano sull’aumentata incidenza dell’edema aritenoideo e sul conseguente ritardato decannulamento.
Il controllo locale dei T1 glottici trattati con radioterapia varia dal 90% al 95% e per i T2 dal 65% al 75%. I risultati del trattamento chirurgico variano dal 95% per i T1 all’80% per i T2. Negli stadi avanzati il controllo locale della chirurgia è del 90% ed i risultati del trattamento combinato chirurgico-radioterapico consentono sopravvivenze libere da malattia a 5 anni del 65%.
I risultati del trattamento dei tumori sottoglottici consentono sopravvivenze a 5 anni di circa il 40%.
Follow- up
I pazienti sottoposti a trattamenti conservativi per carcinomi laringei richiedono follow-up molto stretto al fine di evidenziare precocemente recidive di malattia ulteriormente passibili di trattamento curativo. La chirurgia di recupero della lesione primitiva prevede l’intervento di laringectomia o faringolaringectomia totale nella maggior parte dei casi. Svuotamenti radicali classici e modificati possono consentire il trattamento delle recidive linfonodali. Il follow- up viene condotto a intervalli mensili durante il primo anno, ed in seguito ad intervalli progressivamente più lunghi (2 mesi per il secondo anno, 3-4 mesi per il terzo anno, ogni 6 mesi durante il 4°-5° anno). I controlli proseguiranno in seguito con cadenza annuale o biennale. La radiografia in due proiezioni del torace deve essere effettuata annualmente per poter valutare l’insorgenza di un eventuale carcinoma broncogeno o di metastasi polmonari. In considerazione della possibilità di insorgenza di secondi tumori primitivi metacroni a livello delle alte vie aero-digestive, soprattutto negli stadi III e IV, è utile eseguire annualmente uno studio radiologico dell’ipofaringe-esofago con mezzo di contrasto ed una panendoscopia in narcosi qualora sussista un dubbio clinico (per es. comparsa di sensazione di corpo estraneo, disfagia, otalgia, scialorrea).
Direttive future
Studi clinici randomizzati dedicati alla preservazione d’organo: VALCSG (332 pazienti); EORTC (202 pazienti), GETTEC (68 pazienti). 205 pazienti dei 602 randomizzati sono ancora vivi e liberi da recidiva. Nel 30% dei casi si è preservata la laringe. Per quanto riguarda la sopravvivenza non si è osservata una significativa differenza nei due gruppi tanto da far supporre che un trattamento conservativo, selezionato sulla base della chemiosensibilità, possa rappresentare una valida alternativa alla chirurgia demolitiva. E’necessario sottolineare che questi protocolli sono ancora in fase di sperimentazione clinica.
Bibliografia di riferimento
- Bocca E, Pignataro O, Oldini C. Supraglottic laryngectomy: 30 years of experience. Ann. Oto. Rhinol. Laryn., 92: 14- 18, 1983.
- Chevalier D, Thill C, Darras JA, Piquet JJ. Results of the surgical treatment of cancers of the supraglottic area. Ann. Oto. Laryn. (Paris), 110: 147- 151, 1993.
- Johnson JT, Myers EN, Hao SP, Wagner RL. Outcome of open surgical therapy for glottic carcinoma. Ann. Oto. Rhinol. Laryn., 102: 752- 755, 1993.
- Mendenhall WM, Parsons JT, Stringer SP, et al. Carcinoma of the supraglottic larynx: a basis for comparing the results of radiotherapy and surgery. Head Neck, 12: 208, 1990.
- Million RR, Cassisi NJ. Management of head and neck cancer. A multidisciplinary approach. 2nd Ed. Lippincott Company, Philadelphia 1994.
- Myers EN, Suen JY. Cancer of the head and neck. Ed. WB Saunders Company, Philadelphia 1996.
- Portmann M, Guerrier Y. Traitè de tecnique chirurgicale ORL et cervico- faciale. Ed. Masson & C., Parigi 1987.
- Shah JP. Head and neck surgery. 2nd Ed. Mosby- Wolfe, Barcelona 1996.
- The Department of Veterans Affairs Laryngeal Cancer Study Group. Induction chemotherapy plus radiation compared with surgery plus radiation in patients with advanced laryngeal cancer. New Eng. J. Med., 324: 1685- 1690, 1991.
- Crispino S., Ribecco A., Ghezzi P. Ruolo della chemioterapia nel trattamento del carcinoma della laringe: preservazione d’organo. Argomenti di Oncologia; 19: 15- 20, 1998.
- Lefebvre JL, Wolf G, Luboinski B, et al. Meta-analysis of chemotherapy in head and neck cancer (MACH- NC): (2) Larynx preservation using neoadjuvant chemotherapy (CT) in laryngeal and hypopharyngeal carcinoma. Proc. ASCO, 1473, 1998.
OROFARINGE
OROFARINGE
Cenni di Anatomia
 |
 |
L’orofaringe si estende dalla linea di confine fra palato duro e molle a quella passante nella vallecula glossoepiglottica. È costituito da:
- due pareti laterali, dove si trovano i pilastri tonsillari anteriore e posteriore che racchiudono una zona triangolare dove è alloggiata la tonsilla ed è delimitata in basso dal solco amigdalo- glosso;
- una parete superiore, che comprende la faccia inferiore del palato molle e il velo pendulo;
- una parete anteriore, composta dal terzo posteriore della lingua, o base della lingua, e dalle vallecule;
- una parete posteriore costituita dal piano mucoso e dai muscoli prevertebrali.
Il palato molle con il velo pendulo partecipa all’atto della deglutizione e dell’articolazione dei suoni con modificazioni nella sua estensione e forma. Le pareti laterali che alloggiano le tonsille palatine, organi linfatici, e la base della lingua contribuiscono al passaggio del bolo alimentare che dall’istmo delle fauci viene sospinto indietro e verso il basso nell’esofago, attraverso un passaggio che stabilisce una continuità fra palato molle e parete posteriore. L’epiglottide con il sollevamento della laringe e la prominenza all’indietro della base della lingua chiude l’orifizio laringeo otturandolo e impedendo che frammenti del bolo prendano la via dell’albero respiratorio.
Anatomia Patologica
Come la cavità orale, l’orofaringe è interamente rivestito da mucosa ad epitelio pavimentoso, da cui deriva il 90% dei tumori maligni della regione. La presenza di numerose formazioni ghiandolari salivari minori nel palato molle e di conglomerati linfatici nel tessuto tonsillare giustifica una distribuzione differenziata del restante 10%. Così il 15% dei tumori maligni del palato molle è rappresentato da carcinomi salivari mucoepidermoidi o adenoidocistici e il 10% dei tumori maligni tonsillari da linfomi. Nei carcinomi squamocellulari, a differenza del cavo orale, prevalgono le varianti meno differenziate, inclusi alcuni carcinomi indifferenziati definiti di “tipo rinofaringeo”.
L’evoluzione locale varia a seconda della patologia, con crescita infiltrativa e ulcerativa prevalente nei carcinomi squamosi della regione tonsillare e delle base linguale, crescita espansiva a lungo asintomatica dei tumori ghiandolari del palato o della lingua e dei linfomi tonsillari.
La diffusione per via linfatica è rara nei tumori ghiandolari, estremamente frequente nei carcinomi squamosi (55-65% dei casi), in cui l’adenopatia rappresenta talora l’unico sintomo di malattia. La tonsilla rappresenta inoltre la sede d’origine più frequente delle metastasi linfonodali cervicali cosiddette criptiche, assai spesso scambiate erroneamente con cisti branchiali cancerizzate anche all’esame istologico.
Sintomi ed evoluzione
In fase precoce il sintomo più frequente riferito dai pazienti è costituito da un vago mal di gola. E’ inoltre possibile che il paziente descriva un senso di corpo estraneo in gola che determina difficoltà alla deglutizione. Il dolore può essere anche riferito all’orecchio, quasi sempre unilateralmente. Il trisma è in genere un sintomo tardivo dovuto alla infiltrazione dei muscoli pterigoidei. Anche il tono nasale della voce, l’alito fetido (per ulcerazione e necrosi) e la fissità della lingua sono sintomi tardivi. Un ingrossamento dei linfonodi giugulodigastrici, più frequentemente unilaterale, è molto frequente nei carcinomi della regione tonsillare e della base lingua e può spesso costituire il sintomo di esordio della malattia. Sintomi legati a disseminazione metastatica a distanza della malattia sono, invece, molto rari alla presentazione.
Inquadramento diagnostico
- Visita specialistica ORL (con ispezione e palpazione)
- Panendoscopia
- Biopsia
- RM con mezzo di contrasto (esame di prima istanza)
- TC con mezzo di contrasto
- Rx torace
- Ecografia epatica
- Esami del sangue completi
Classificazione in categorie di T (UICC, 1997)
- Tx primitivo non definibile
- T0 primitivo non evidenziabile
- Tis carcinoma in situ
- T1 dimensioni massime <=2 cm
- T2 dimensioni massime comprese fra 2 e 4 cm
- T3 dimensioni massime >4 cm
- T4 sono invase strutture adiacenti, ad es. muscoli pterigoidei, mandibola, palato duro, muscoli profondi della lingua, laringe La classificazione delle adenopatie è la stessa usata per le altre localizzazioni.
Modalità terapeutiche
Chirurgia
In lesioni limitate (T1) sono possibili interventi conservativi, in genere di elettroexeresi per via transorale (velopendulo, tonsilla) o, in sedi più profonde (base linguale) per via faringotomica laterale. Nel caso di neoplasie più estese gli interventi sono più demolitivi, con conseguenze funzionali più o meno pesanti; di tipo diverso a seconda della sede del tumore e della sua estensione. Nelle neoplasie della regione tonsillare (o amigdalo- glosso- palatina) a sede laterale la chirurgia comporta spesso accessi transmandibolari e ricostruzioni complesse, con impegno sostanziale della funzione deglutitiva e masticatoria e alterazioni estetico- morfologiche.
Gli interventi più radicali comportano la resezione della regione tonsillare e delle parti adiacenti del palato molle e della lingua per via transmandibolare (per lo più demolitiva dell’osso), la resezione di gran parte della base della lingua.
In quelle più posteriori, in genere mediane (base della lingua, regione glossoepiglottica) sono più spesso coinvolte strutture laringee (epiglottide, spazio tireoepiglottico) e interventi che implicano laringectomie parziali o totali) e quindi disturbi della funzione fonatoria: la laringectomia sopraglottica allargata alla base linguale, la subglosso- laringectomia totale, fino alla glosso- laringectomia totale.
In tutti i casi si rendono necessari svuotamenti delle logge linfatiche cervicali con tecnica variabile a seconda delle caratteristiche delle adenopatie, da eseguirsi mono- o bilateralmente secondo la sede del tumore primitivo, quasi sempre in concomitanza e in continuità con quest’ultimo.
Si tratta comunque di approcci chirurgici complessi, con vari gradi di difficoltà, non realizzabili in tutti i reparti di chirurgia ORL o maxillo-facciale. I risultati in termini di guarigione sul piano oncologico sono soddisfacenti anche in forme molto estese. Il prezzo pagato in termini di qualità di vita può apparire elevato, anche se si è alquanto ridotto negli ultimi anni con il miglioramento delle procedure ricostruttive. Esso giustifica la continuazione degli sforzi per ricercare trattamenti alternativi più conservativi ma non la pervicacia nel perseguire questo obiettivo.
Radioterapia
Il trattamento standard viene eseguito in genere per via transcutanea, utilizzando campi contrapposti e dosi comprese fra i 60 e i 70 Gy con frazionamento convenzionale (v. tabella pag. 42).
Sensibili progressi sono stati ottenuti nei carcinomi della base linguale di limitata o media estensione (T1-T2) con l’impiego della brachiterapia interstiziale supplementare ad una irradiazione esterna condotta a dosi appropriate. Per il resto sono stati saggiati in campo radioterapico trattamenti condotti con diverse modalità di frazionamento delle dosi o/ e di combinazioni con farmaci radiosensibilizzanti o/ e antiblastici.
Molte delle nuove strategie si prefiggono anche di cercare di ottenere uguali o migliori risultati di quelli ottenibili con terapie convenzionali con il massimo risparmio dell’organo, in questo caso l’orofaringe, e delle strutture adiacenti, al fine di assicurare il migliore risultato sotto il profilo oncologico con la migliore qualità di vita possibile.
Accenniamo di seguito ad alcune terapie che più sono state oggetto di studio e che spesso trovano una applicazione presso i centri specialistici di oncologia radioterapica e medica.
Tutte le sedi eccetto la base della lingua. Per gli stadi T2- 3 N0/N1 (>3 cm)
La radioterapia iperfrazionata alla dose per frazione di 1.2 Gy x 2 frazioni al di, con intervallo di 6 ore per una dose totale di 80.5 Gy (EORTC 22791) ha comportato un controllo locale del 56% a 5 anni con differenza significativa rispetto a casi analoghi trattati con frazionamento convenzionale della dose (38%). I dati di sopravvivenza a 5 anni del 40% della serie iperfrazionata rispetto a quella trattata con frazionamento convenzionale (30%) non sono risultati significativamente diversi, ma presentano una evidente tendenza ad un migliore risultato.
Tutte le sedi, stadi III e IV
Sono stati condotti molti studi di radioterapia con frazionamenti alterati che ancora non hanno messo in evidenza sicuri risultati almeno nel controllo locale della malattia.
Il tipo di frazionamento alterato che ha dato i migliori risultati nei tumori maligni in stadio avanzato dell’orofaringe è stato un frazionamento bigiornaliero con 1.6 Gy per frazione e dose totale di 70 Gy. L’intervallo fra le frazioni deve essere di almeno 6 ore. I migliori risultati in termini di controllo locale e di sopravvivenza a 5 anni sono stati riportati da Wang in uno studio non randomizzato e tale frazionamento è oggi oggetto di studi randomizzati per avere la conferma della sua validità. Una ulteriore opzione terapeutica è l’associazione di radioterapia e chemioterapia. E’ possibile che le due armi terapeutiche combinate migliorino i risultati, specie se usate in modo concomitante anche se costituiscono una terapia piuttosto pesante per gli effetti collaterali. L’associazione più usata prevede per la chemioterapia schemi di trattamento con derivati del platino (cisplatino o carboplatino) e 5-fluorouracile.
Gli studi attualmente in corso, che non sono ancora stati pubblicati e che potrebbero evidenziare opzioni terapeutiche per migliori risultati sono i seguenti:
- Studio italiano multicentrico randomizzato (ORO- 93) nel quale vengono confrontate la radioterapia convenzionale da sola (seguita da chirurgia di salvataggio se necessaria) radioterapia bifrazionata con iperfrazionamento accelerato secondo Wang (1.6 Gy x 2 volte al giorno, dose totale di 70 Gy e intervallo programmato) e la radioterapia convenzionale concomitante a chemioterapia (tre cicli alla prima, quinta e nona settimana con carboplatino e 5Fluorouracile). Tale studio, per gli ultimi due anni, è stato condotto sotto l’egida del Progetto Finalizzato CNR.
- Studio condotto dall’RTOG (Radiation Therapy Oncology Group): è uno studio di fase III, RTOG 90-03, che include neoplasie epiteliali della cavità orale, dell’orofaringe compresa la base della lingua, dell’ipofaringe e laringe sovraglottica e confronta il frazionamento convenzionale della dose verso due tipi di iperfrazionamento accelerato.
Strategia terapeutica
Le terapie di scelta sono rappresentate da: chirurgia e radioterapia, da sole o combinate, e dalla chemioterapia, utilizzata sempre in combinazione con le precedenti in varie sequenze. Le varie opzioni terapeutiche possono essere considerate diversamente a seconda che siano consolidate dalla pratica clinica o siano ancora da testare con studi clinici controllati. Utilizzando quanto già noto e collaudato, è possibile riportare sinteticamente in una tabella l’elenco delle indicazioni consigliabili come terapia standard tenendo presente che i risultati di vari studi attualmente in corso potrebbero modificare significativamente l’orientamento.
Terapia Standard
 * Nelle lesioni più estese rimangono in opzione trattamenti multidisciplinari programmati (RT + CT concomitanti; ERT preoperatoria)
* Nelle lesioni più estese rimangono in opzione trattamenti multidisciplinari programmati (RT + CT concomitanti; ERT preoperatoria)
Controlli periodici dopo la terapia
Fino a due mesi dalla fine del trattamento sono consigliabili visite periodiche in tempi diversi da paziente a paziente, ma comunque a breve distanza, per la verifica della guarigione della ferita chirurgica o delle reazioni acute da radioterapia.
Dopo questa prima fase si consigliano:
- a due mesi dalla fine della terapia, la visita clinica ed esami di diagnostica per immagini (RM o TC) per valutare la risposta clinica al trattamento;
- visite periodiche ogni 3 mesi durante il primo e secondo anno, con esami di diagnostica per immagini (RM o TC) due volte l’anno;
- visite periodiche ogni 4 mesi durante il terzo anno, con esami di diagnostica per immagini (RM o TC) due volte l’anno;
- visite periodiche ogni 6 mesi durante il quarto e quinto anno, con esami di diagnostica (RM o TC) una volta l’anno;
- visite periodiche con frequenza annuale o biennale per tutta la vita del paziente.
Risultati: controllo loco- regionale e sopravvivenza a 5 anni
In linea generale è possibile affermare che negli stadi iniziali di malattia (T1- 2/ N0) le possibilità di guarigione con radioterapia o chirurgia non demolitiva, da sole, oscillano fra l’80% e il 70%, per tutte le localizzazioni orofaringee.
Negli stadi più avanzati per estensione locale (T3- T4) o regionale (N1- 2-3) le possibilità di sopravvivenza a 5 anni si riducono nettamente e progressivamente con l’avanzare dello stadio andando dal 50% al 20% a seconda del trattamento eseguito. La riduzione è nettissima per i casi trattati con la sola radioterapia transcutanea (20-22%), mentre il controllo locoregionale varia dal 55% al 60% per i casi trattati con chirurgia demolitiva (raramente da sola, quasi sempre associata a RT postoperatoria).
Tra i fattori prognostici più importanti, oltre alla estensione locale, figurano l’estensione delle metastasi linfonodali (sia per numero e dimensioni, che per livello), e l’adeguatezza del trattamento (grado di radicalità chirurgica, dosi e campi di RT). Altro fattore importante è la caratteristica infiltrante della neoplasia primitiva, soprattutto nello sconfinamento nella base linguale e nei tessuti parafaringei.
Fattori prognostici
I principali fattori prognostici dei carcinomi dell’orofaringe sono rappresentati dall’estensione del tumore primitivo (da T1 a quella T4) e dall’entità del coinvolgimento dei linfonodi regionali (da N0 a N1- 3); il grado di interessamento linfonodale è, forse, il più significativo tra i fattori correlati al mancato successo del trattamento. La sede di presentazione della neoplasia può rivestire anch’essa un valore prognostico: le neoplasie a sede tonsillare sono generalmente considerate a migliore prognosi rispetto a quelle della base lingua o della parete posteriore; l’estensione al solco glosso- epiglottico implicherebbe una prognosi più severa. Le scadenti condizioni generali, un basso performance status, il sesso maschile costituirebbero ulteriori fattori prognostici sfavorevoli anche se di minore rilievo.
Bibliografia di riferimento
- Gwozdz J. T., Morrison W. H., Garden A. S., et al. Concomitant boost radiotherapy for squamous carcinoma of the tonsillary fossa. Int. J. Radiat. Oncol. Biol. Phys., 39: 127- 135, 1997
- Horiot J. C., Le Fur R., N’Guyen T., et al. Hyperfractionation versus conventional fractionation in oropharyngeal carcinoma: final analysis of a randomized trial of the EORTC Cooperative Group of Radiotherapy. Radiother. Oncol., 25: 231- 241, 1992
- Olmi P., Fallai C., Rossi F., et al. Conventional radiotherapy versus accelerated hyperfractionated radiotherapy versus conventional radiotherapy and concomitant chemotherapy in advanced oropharyngeal carcinoma: a randomized clinical trial (Abstr.) Eur. J. Cancer, 31 (suppl. 5) S91, 1995
- Housset M., Baillet F., Dessard- Diana B. et al. A retrospective study of three treatment techniques for T1- T2 base of tongue lesions: surgery plus postoperative radiotherapy, external radiation plus interstitial implantation, external radiation alone. Int. J. Radiat. Oncol. Biol. Phys., 13: 511- 516, 1987
- Wang C. C., Montgomery W., Efird J. Local control of oropharyngeal cacinoma by irradiation alone. Laryngoscope, 529- 533, 1995
- Kraus D. H., Vastola A. P., Huvos G., Spiro R. H. Surgical management of squamous cell carcinoma of the base of the tongue. Am. J. Surg., 166: 384- 389, 1993
- Fein D. A., Lee W. R., Amos W. R. et al. Oropharyngeal carcinoma treated with radiotherapy: a 30 years experience. Int J. Radiat. Oncol. Biol. Phys, 34: 289- 296, 1996
- Lefebvre J. L., Vankemmel B., Prevost B. et al. Composite resection with mandibulectomy in the treatment of posterolateral oral cavity and lateral oropharynx squamous cell carcinoma. Am. J. Surg., 166: 435- 439
- Gehanno P., Depondt J., Guedon C., et al. Primary and salvage surgery for cancer of the tonsillar region: a retrospective study at 120 patients. Head and Neck, 15: 185- 189, 1993
- Zelewsky M. J., Harrison L. B., Fass D. E. et al. Postoperative radiation therapy for squamous cell carcinoma of the oral cavity and oropharynx: impact of therapy on patients with positive surgical margins. Int. J. Radiat. Oncol. Biol. Phys., 2: 17- 21, 1993